






こちらのページでは中和について解説していきます。
イラストや図を用いてわかりやすく解説していくので授業の予習復習や定期テスト対策にご活用ください!
その他のやる気アシストの勉強記事 (理科編) もこちらから見ることができます。ぜひご覧ください!
酸性の物質とアルカリ性の物質を混ぜ合わせると、お互いの性質を打ち消し合う反応が起きます。これを中和といいます。今回は、さまざまな中和の例をご紹介していきます。
その前に、酸性・アルカリ性ってなんだっけ?と思った方はこちらの記事で詳しく解説しておりますのでぜひご覧ください!
それでは、まずは塩酸と水酸化ナトリウムの中和から見ていきましょう。
水酸化ナトリウム水溶液にBTB液を加えると、水溶液の色は青色になりました。ここにピペットを用いて塩酸を加えると、ある量を加えたところで水溶液が緑色になりました。さらに塩酸を加えると、水溶液は黄色になりました。

この実験で中性になった水溶液を蒸発皿に取って下から加熱しました。すると、水溶液は蒸発して最終的に白い結晶が残りました。これは次の化学変化の結果を表しています。
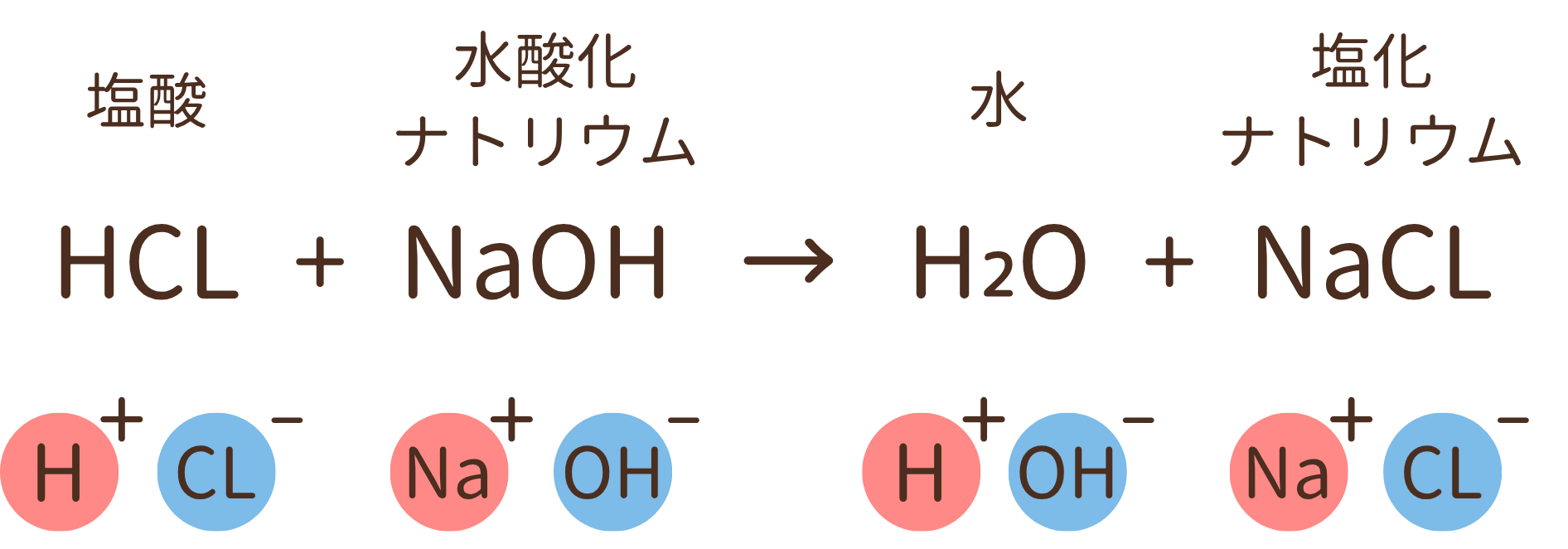
酸性やアルカリ性の性質は、それぞれ 水中で生じる特定のイオン によって決まります。酸性は 水素イオン(H⁺) ,アルカリ性は 水酸化物イオン(OH⁻) がそれぞれの性質のもととなっています。
二酸化炭素は弱い酸性を持っています。つまり炭酸水は酸性の水溶液です。水酸化カルシウム水溶液は石灰水とも呼ばれます。これはアルカリ性の水溶液です。2つを混ぜ合わせたときの反応を見ていきましょう。
炭酸水・水酸化カルシウム水溶液の化学式はそれぞれH₂CO₃・Ca(OH)₂です。
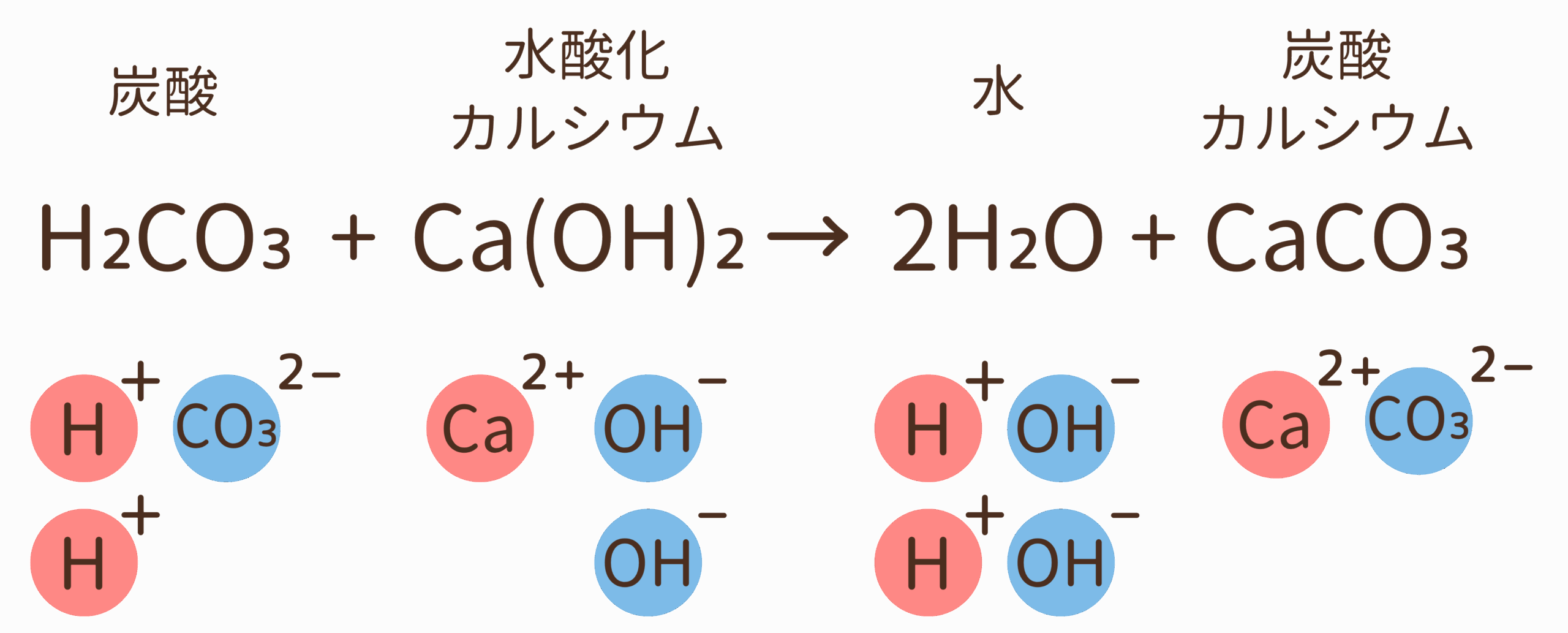
炭酸水と水酸化カルシウム水溶液を混ぜ合わせると白濁が生じます。これは炭酸カルシウムが発生したことを表しています。
硫酸は強い酸性、水酸化バリウムはアルカリ性の白い粉末です。硫酸の化学式はH₂SO₄・水酸化バリウムの化学式はBa(OH)₂ です。
2つを混ぜ合わせたときの反応を見ていきましょう。
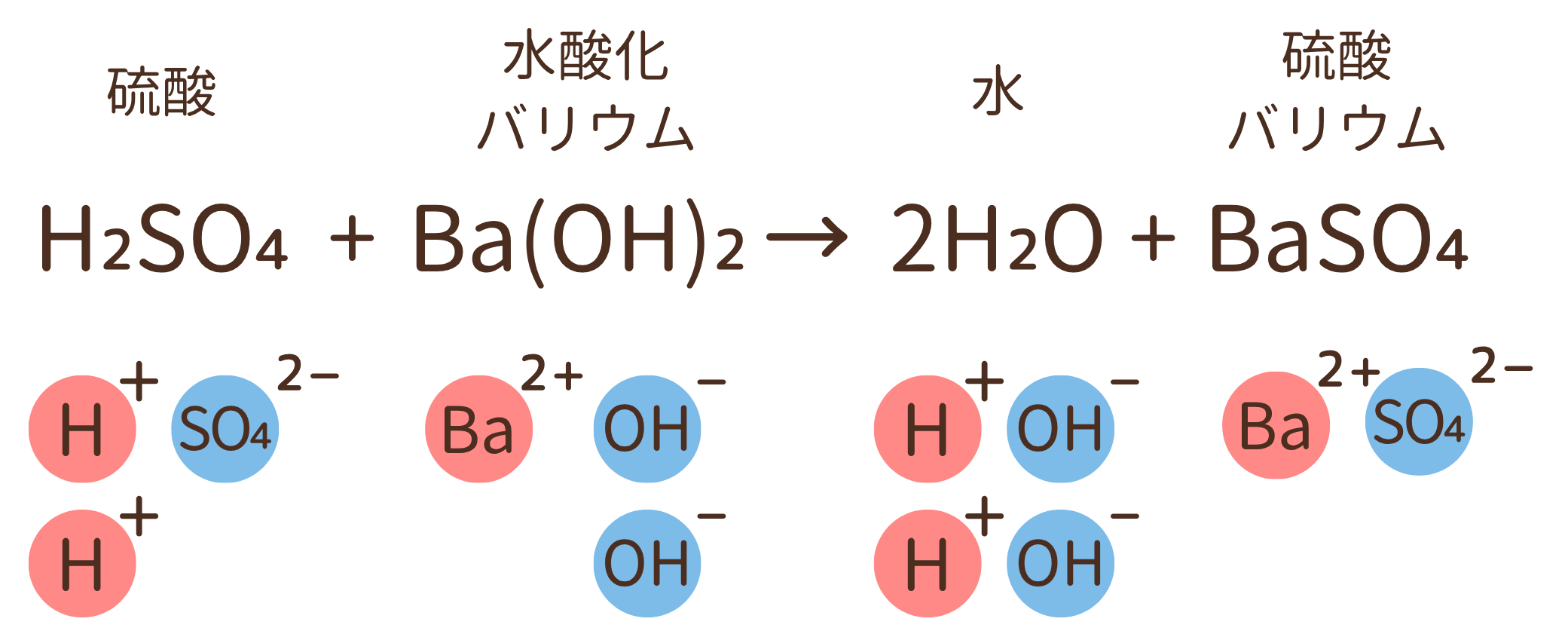
中和反応によって、水以外に生じる物質のことを塩(えん) と呼びます。
塩酸と水酸化ナトリウムの中和で発生する塩化ナトリウム
炭酸水と水酸化カルシウムの中和でできる炭酸カルシウム
硫酸と水酸化バリウムの中和でできる硫酸バリウム
これらはすべて塩に該当します。
\小・中・高校生の勉強にお悩みのある方へ/

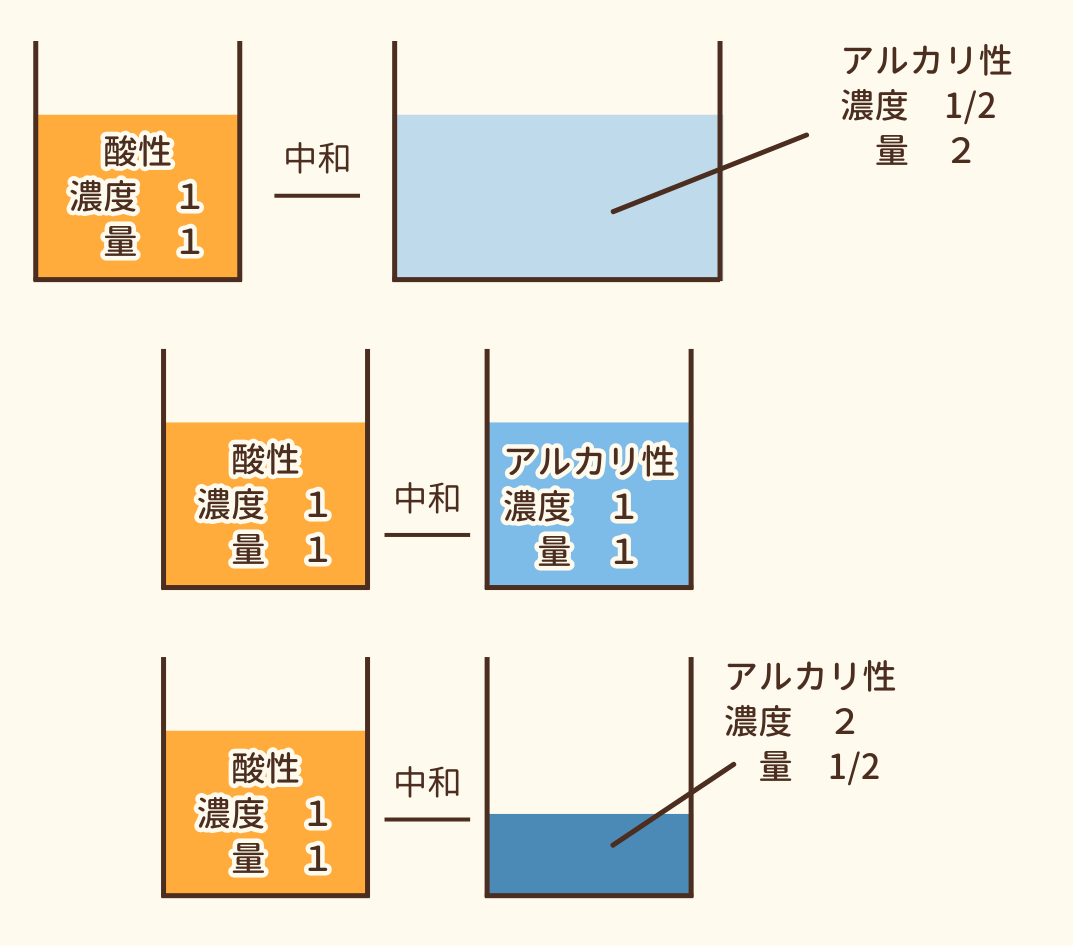
酸とアルカリを中和して中性になるときには、酸の水素イオン(H⁺)の数とアルカリの水酸化物イオン(OH⁻)の数は等しいです。
また、濃さが2倍のときは量は1/2倍、濃さが1/2倍のときは量が2倍で中性になります。下の図で確認しましょう。
最後までお読みいただきありがとうございました。
今回は電気分解について紹介しました。その他の理科の定期テスト対策の記事はこちらからチェックしてみてください!
他にも様々なお役立ち情報をご紹介しているので、ぜひご参考にしてください。質問などございましたら、お気軽にお問い合わせください!



