







こちらのページでは原子の構造とイオンについて解説していきます。
イラストや図を用いてわかりやすく解説していくので授業の予習復習や定期テスト対策にご活用ください!
その他のやる気アシストの勉強記事 (理科編) もこちらから見ることができます。ぜひご覧ください!
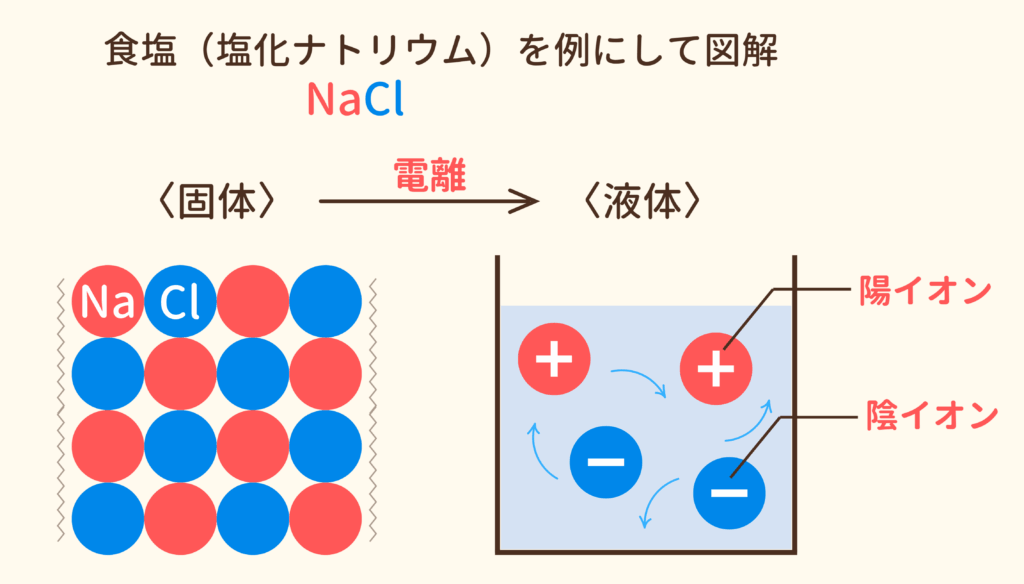
電解質は、水に溶かすとプラスの電気を持った粒子とマイナスの電気を持った粒子に分かれます。(この現象を電離といいます。)
※電解質について詳しく知りたい方はこちらから!
電気を帯びた粒子はイオンと呼ばれ、プラスのイオンは陽イオン、マイナスのイオンは陰イオンと呼ばれます。
固体のときはイオンは結晶に固定されて動けませんが、水に溶かすと水分子に囲まれて安定化し、自由に動けるようになります。この自由に動くイオンの移動によって電気が流れます。
イオンの発生は、原子の構造と関係しています。原子は下図のような構造をしています。
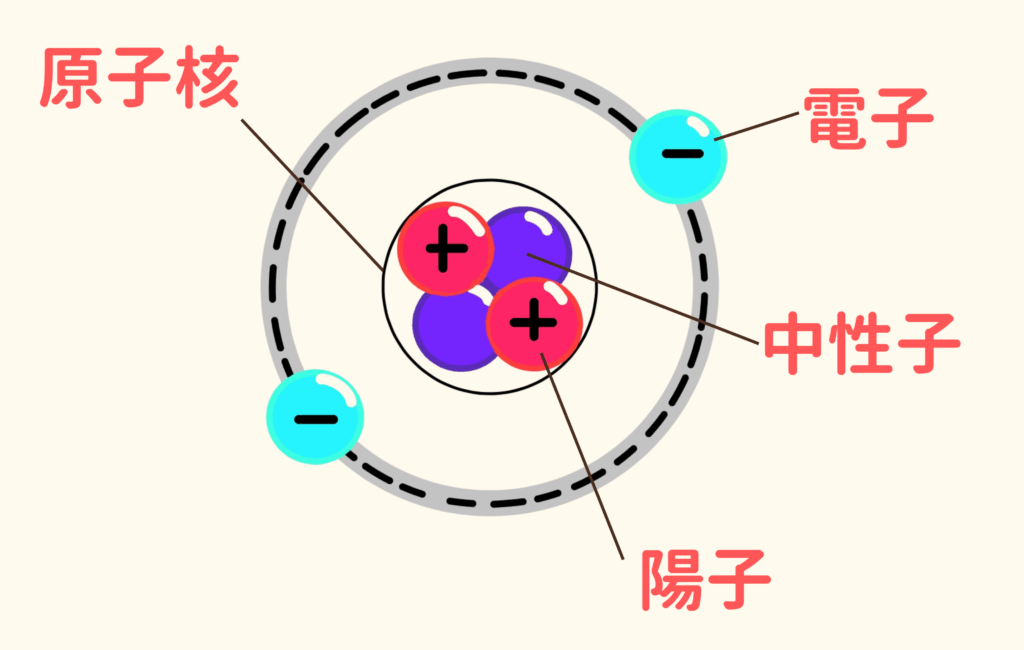
原子は、原子核とその周りを飛ぶ電子から成り立っています。原子核には陽子と中性子があります。陽子は+の電気、電子は-の電気を持っています。
原子の構造の特徴
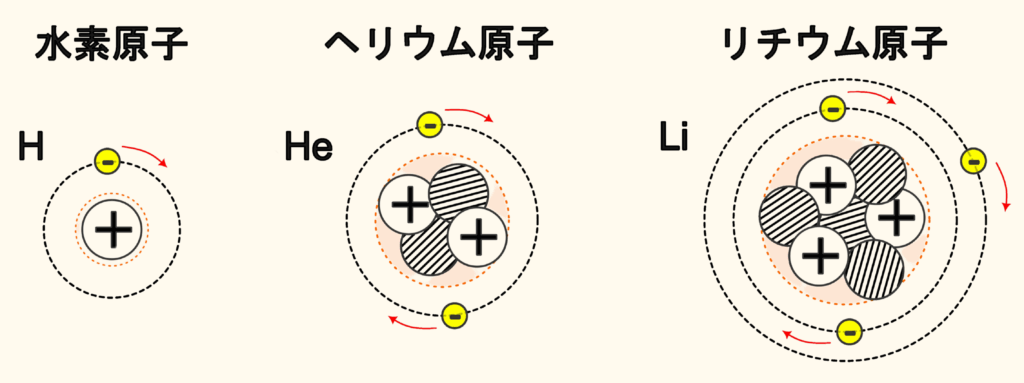
原子には、下図のように陽子と電子の数は元素によって決まっています。
イオンは、下図のように原子内の電子が出たり入ったりすることで生まれます。電子が出ていくことで+の電気になる原子は陽イオン、入ってくることで-の電気になる原子は陰イオンといいます。陽イオンになるか陰イオンになるかは、原子の種類によって決まっています。
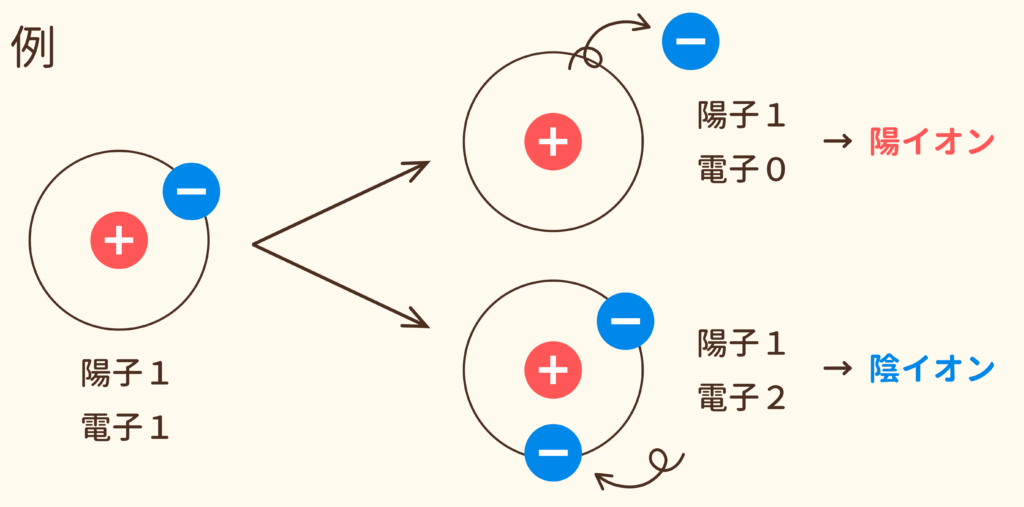
原子の特徴にあったように、陽子・電子の数は元素によって異なります。しかし、同じ原子内の陽子と電子の数は同じです。なので、原子全体として電気は持っていません。
\小・中・高校生の勉強にお悩みのある方へ/

電子をいくつ失う・受け取るかは、原子の種類によって決まっています。例えばナトリウム(Na)は、イオンになった時に1つ電子を失って陽イオンになります。塩素(Cl)は、イオンになった時に1つ電子を受け取って陰イオンになります。この時、ナトリウムイオンの表記はNa⁺、塩化物イオン(塩素がイオンになった時の呼び名です)はCl⁻と表記します。
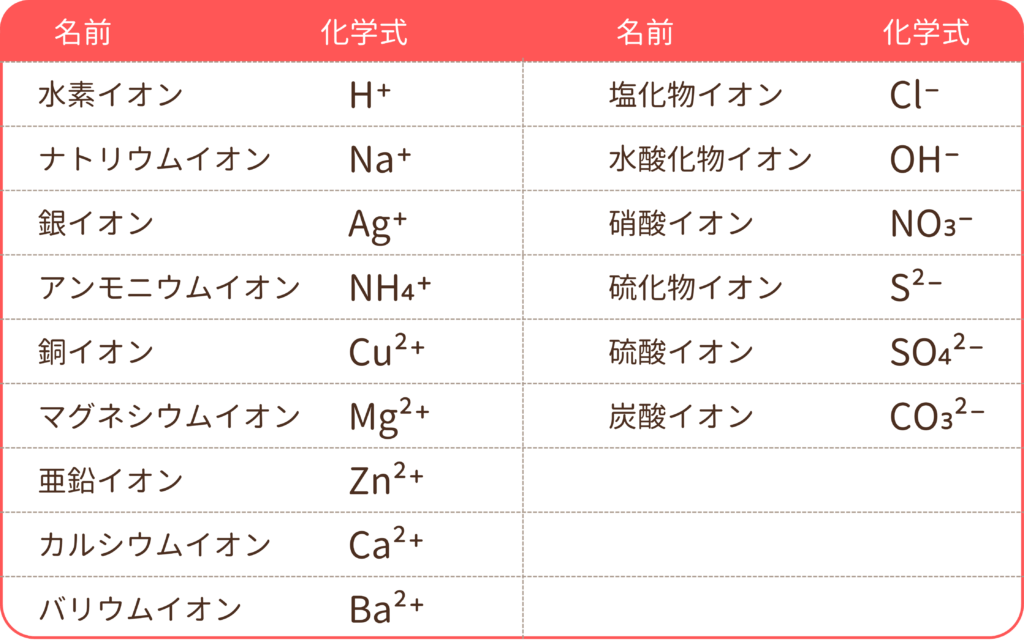
代表的なイオンの種類とそれを表す化学式を下の表にまとめました。
最後までお読みいただきありがとうございました。
今回は電気分解について紹介しました。その他の理科の定期テスト対策の記事はこちらからチェックしてみてください!
他にも様々なお役立ち情報をご紹介しているので、ぜひご参考にしてください。質問などございましたら、お気軽にお問い合わせください!



